Terapia Génica

Líneas de investigación
Contenidos con Investigacion .
Terapia Génica
Nuestro grupo está centrado en (i) la investigación de los mecanismos subyacentes a distintos tipos de tumores huérfanos y enfermedades raras y (ii) la búsqueda de nuevas estrategias terapéuticas para combatir las enfermedades raras.
Nuestras líneas de investigación están actualmente enfocadas en los tumores de la granulosa ovárica asociados a FOXL2, la leucoencefalopatía agresiva precoz relacionada con KARS1 y en las distrofias musculares congénitas asociadas a LMNA. En todos los casos el editado génico mediado por CRISPR es la aproximación terapéutica mayormente seleccionada.
Contamos con la siguiente financiación:
- Evolución de estrategias terapéuticas basadas en CRISPR/Cas con potencial para el tratamiento de la distrofia muscular congénita asociada a LMNA (PI23CIII/00041). Acción Estratégica en Salud Intramural ISCIII 2023. IP: Ignacio Pérez de Castro. 2025-27. 138000€.
- La vía de los glucocorticoides en la distrofia muscular congénita relacionada con LMNA: Descifrando mecanismos y probando estrategias terapéuticas (PID2023-147678OB-I00). Proyectos Generación de Conocimiento AEI 2023. IP: Ignacio Pérez de Castro. 2025-27. 275000€.
- Investigating the potential of Replacement Gene Therapy for Early-Onset Progressive Leukoencephalopathy using iPSCs and a Kras1 knock-in mouse model. Cure KARS Laia Foundation. IP: Ignacio Pérez de Castro. 2025-28. 250000€.
- Distrofias congénitas asociadas a LMNA. LCMD-Research Foundation. IP: Ignacio Pérez de Castro. 2026-27. 43000€.
Publicaciones destacadas
The RD-Connect Registry & Biobank Finder: a tool for sharing aggregated data and metadata among rare disease researchers. Eur J Hum Genet. 2018 May;26(5):631-643
Gainotti S, Torreri P, Wang CM, Reihs R, Mueller H, Heslop E, Roos M, Badowska DM, de Paulis F, Kodra Y, Carta C, López-Martín E, Miller VR, Filocamo M, Mora M, Thompson M, Rubinstein Y, Posada de la Paz M, Monaco L, Lochmüller H, Taruscio D.
PUBMED DOIContenidos con Investigacion .
-

-

-

-

María Luisa Martínez Fernández
Técnico Superior Especializado de OPI
Código ORCID: 0000-0001-8615-0226
-
-

-

-

Listado de personal
Información adicional
- Tesis doctorales:
- Paula Estebán (en proceso desde 2025; UNED-ISCIII). Búsqueda de estrategias terapéuticas para el tratamiento de la leucoencefalopatía progresiva de aparición temprana asociada a mutaciones en KARS1.
- Silvia Méndez (en proceso desde 2024; UNED-ISCIII). La vía de los glucocorticoides en la distrofia muscular congénita relacionada con LMNA: Descifrando mecanismos y probando estrategias terapéuticas.
- Mario Santafé Méndez (en proceso desde 2024; UNED-ISCIII). Estudio del potencial de los editores de bases para el tratamiento de las distrofias musculares congénitas asociadas a LMNA.
- Sandra Amarilla (en proceso desde 2020; UNED-ISCIII). Papel de FOXL2-C134W en tumores de granulosa ovárica.
- Déborah Gómez-Domínguez (2024; U. Autónoma de Madrid). Estudio del potencial de la tecnología CRISPR en el tratamiento de las distrofias musculares congénitas asociadas a LMNA.
- Trabajos de fin de Máster:
- Adrián Martínez-Fernández (2025; U Autónoma de Madrid). CRISPR- and dTAG-Mediated Specific Targeting of LMNAR249W in human myoblasts.
- Mario Santafé (2024). Use of base editing for the treatment of LMNA-related congenital muscular dystrophy.
- Davide Mazzeo (2024). Investigating the Impact of Adenine Base Editing for the treatment of the LMNA-congenital muscular dystrophy: A Comprehensive Molecular and Phenotypic Analysis.
- Ana María Quintana Prego (2022). Uso de base editing para el tratamiento de la distrofia muscular congénita asociada a LMNA.
- Fernando Gómez García (2021). Eliminación específica de la mutación Lmna-R249W mediante CRISPR/Cas9 en fibroblastos embrionarios de ratón.
- Alba Cano Bustos (2021). Caracterización y modelización de la mutación de lamina C R264C de una laminopatía en Drosophila melanogaster.
- Naroa Martín (2020). Estudio del inhibidor ARRY-797 como nueva estrategia terapéutica para la distrofia muscular congénita asociada a LMNA (L-CMD).
- Sarai Araujo (2019). Análisis del papel de TRMT61B, una metil-transferasa de ARN, en la regulación de la expresión del genoma mitocondrial en células tumorales.
- Laura Alonso (2019). Study of MEK1/2 and NAT10 inhibitors as a novel therapeutic approach for LMNA-associated congenital muscular dystrophy.
- Alejandra Ramos (2019). Estudio genético de la función de la mutación 402C>G de FOXL2, mediante el uso de CRISPR/Cas9, y su contribución al desarrollo de tumores de células de la granulosa.
- María Jiménez Aguirre (2018). Bioinformatic search for an aneuploidy-related signature with prognostic value in cancer.
- Martín Salamini (2018). Analysis of the biological function of TRMT61B in a chromosomal instability context.
- Déborah Gómez Domínguez (2018). Caracterización de mioblastos de ratón con mutaciones en LMNA inducidas mediante CRISPR/Cas9.
- Trabajos de fin de Grado:
- Marta García de la Fuente (2023). Estudio del potencial de los editores de bases en fibroblastos de ratón para el futuro tratamiento de la distrofia muscular congénita asociada al gen LMNA.
- Antonio Rochano (2022). Estudio funcional de la mutación de lamina C R264W en un modelo de laminopatía en Drosophila melanogaster.
- Diego Moneo (2020). La inhibición de NAT10 como posible enfoque terapéutico para la distrofia muscular congénita asociada al gen LMNA.
- Andrea González Vicario (2018). Edición génica con CRISPR/Cas9 como estrategia terapéutica en cáncer de ovario de células de la granulosa.
- Paula Maiayeh (2017). Edición génica mediada por CRISPR/CAS9 administrado a través de diferentes formatos.
- Marta Cadenas (2017). Edición génica mediada por CRISPR/Cas9 en el gen LMNA.
- Irene Hernández (2017). Efecto de la actividad específica CRISPR/Cas9 en células tumorales de la granulosa ovárica.
- PATENTES:
Makers: María José Bueno 1,2, Ignacio Pérez de Castro 1, José Fernández-Piqueras 2,Marcos Malumbres 1 1 Centro Nacional de Investigaciones Oncológicas (CNIO); 2 Universidad Autónoma de Madrid
Title: "Uso del Microrna-203 y de Sistemas de Expresión del mismo para fabricar medicamentos contra el cáncer" (Uses of the miRNA203 and its expression systems in the generation of antitumoral drugs). Identification number (Spain): P200800739. Priority Country: SPAIN.Owner's Institution: Fundación Centro Nacional de Investigaciones Oncológicas Carlos III.
El Programa de Enfermedades Raras sin diagnostico – SpainUDP se desarrolla desde el Instituto de Investigación de Enfermedades Raras (IIER), perteneciente al ISCIII.
Dicho Programa intenta dar respuesta al elevado número de consultas que este centro viene recibiendo desde hace años sobre casos de enfermedades raras sin diagnóstico. SpainUDP ofrece un enfoque multidisciplinario a aquellos pacientes que llevan un prolongado periodo de tiempo buscando sin éxito un diagnóstico para su enfermedad.
¿Cómo contactar para solicitar entrar en el programa?
Existen dos posibilidades de acceso a este programa:
1. Registrándose en el registro de pacientes de enfermedades raras http://registroraras.isciii.es dejando la pestaña de diagnóstico como caso sin diagnóstico
2. A través del Sistema de Información y Orientación de Enfermedades Raras de FEDER
También se puede iniciar el primer contacto a través del correo registroraras@isciii.es
Este programa se realiza bajo la estrecha colaboración con la Red Internacional de Casos sin Diagnósticos (UDNI), la federación Española de Enfermedades Raras (FEDER), la Asociación D'Genes y la Asociación Objetivo Diagnóstico, cuyo Facebook puede seguirse en este enlace https://www.facebook.com/objetivodiagnostico/
Descripción del proceso
Análisis fenotípico
Durante la primera fase del protocolo se lleva a cabo un análisis del fenotipo clínico. Para ello:
· Se solicita la información clínica disponible de cada caso y todos los documentos son cuidadosamente revisados por los profesionales del Programa. La información clínica de los pacientes se almacena de forma segura en el Registro Nacional de Enfermedades Raras, previa firma del correspondiente consentimiento informado.
· Se establece una estrecha colaboración con los servicios médicos locales que atienden a los pacientes
· Si es necesario, los pacientes admitidos en el programa son citados en consultas externas, o bien ingresados en el Hospital Universitario Puerta de Hierro de Majadahonda (Madrid) para realizar un estudio clínico detallado de dichos pacientes, así como las pruebas diagnósticas que se consideren necesarias para completar la valoración de su estado clínico
Estudios genéticos
· Durante esta fase, toda la información procedente de los estudios genéticos realizados en otros centros es analizada, llegando en caso de considerarlo necesario, a contactar con el laboratorio que ha llevado a cabo dicho estudio genético con el objetivo de validar conjuntamente tanto los hallazgos como la falta de los mismos.
· Cualquier decisión acerca de decisiones a tomar sobre repetición/comprobación de análisis ya realizados, se lleva a cabo en estrecha colaboración con la familia, pero también con sus médicos.
· Por último, si el caso lo requiere se procede a realizar un estudio del exoma completo del caso, de los padres y si lo consideramos de interés en los hermanos del caso. Para este análisis se requiere la firma de un nuevo consentimiento informado ad hoc para estudios de este tipo.
· Para la realización del exoma, se requieren muestras de sangre, muestras que se obtienen siguiendo el procedimiento estandarizado por el Biobanco Nacional de Enfermedades Raras ISCIII (BioNER), con la consiguiente firma de un consentimiento informado que permite guardar la parte de la muestra no utilizada en el diagnóstico en el propio biobanco. Estas muestras podrán ser utilizadas para comprobaciones de análisis diagnósticos y para estudios funcionales demostrativos de que la mutación(es) encontrada(s) son la causa de la enfermedad.
Fase de información
· El informe completo del exoma es enviado tanto al médico del caso como a la propia familia. Los médicos de cada caso son los que finalmente proceden a valorar los hallazgos, los discuten con el IIER, si lo consideran necesario, y son los encargados de transmitir y firmar el diagnóstico definitivo al caso o a la familia (en caso de menores o incapacitados).
· El informe genético se envía a la familia para que puedan entregarlo en caso de terceras opiniones o desplazamientos de lugar de residencia.
¿Qué pasa si el estudio del exoma no detecta ninguna mutación capaz de relacionarse con el cuadro clínico?
Aproximadamente 1 de cada dos estudios de este tipo se encuentra en esta situación, es decir, no se alcanza un diagnóstico claro. Para ello se está colaborando con la Red Internacional de Casos sin Diagnóstico http://www.udninternational.org/ y con los proyectos europeos RD-CONNECT y SOLVE-RD, recientemente aprobado precisamente para ver la manera de solucionar el diagnóstico de estas personas entre todos.
La idea es buscar casos similares en todo el mundo, a través de la compartición de datos del fenotipo clínico – debidamente mapeado con la Ontología de Fenotipo Humano – y datos de variantes genéticas candidatas. Todo este vasto proceso, que está comenzando a lanzarse muy recientemente a través de plataformas de intercambio seguras como Phenome Central, Matchmaker Exchange y desde RD-CONNECT permitirá abordar diferencias y similitudes entre casos de distinto origen, permitirán conocer mejor los mecanismos de las enfermedades complejas y facilitará el diagnóstico de muchos más casos.
Servicio de Información Telefónica para la Embarazada (SITE)
Teléfono: 91 822 24 36 (para la población general).
Horario de consultas: 9 a 15 horas (lunes a viernes)

La información que se ofrece en el SITE está especialmente dirigida a:
- Las mujeres embarazadas y sus parejas.
- Las parejas que planean una gestación.
- Los padres que han tenido previamente un hijo (o un embarazo) con algún defecto congénito.
En este servicio se puede consultar sobre el riesgo que para defectos congénitos puede implicar la exposición a cualquier factor u otros aspectos que les puedan preocupar a ese respecto (tales como: edades de los padres, tabaco, alcohol, drogas, exposiciones laborales maternas o paternas, contacto con animales domésticos, etc). Para problemas médicos o tratamientos, la consulta debe realizarla el profesional encargado del cuidado de la paciente.
En cada llamada, además se ofrece información general sobre medidas preventivas para defectos congénitos, que se envía por correo a todas aquellas personas que lo soliciten.
Servicio de Información Telefónica sobre Teratógenos Español (SITTE)
Teléfono: 91 822 24 35 (para profesionales sanitarios).
Horario de consultas: 9 a 15 horas (lunes a viernes)

Este servicio tiene una finalidad equivalente a la del SITE, pero está dirigido a profesionales de la salud. Todas las consultas sobre problemas médicos o tratamientos deben ser canalizadas a través del SITTE.
Se conoce como enfermedad rara (ER) aquella cuya prevalencia es inferior a 5 casos por cada 10.000 personas en la Comunidad Europea. El objetivo del Registro de Pacientes de Enfermedades Raras es ofrecer a los profesionales del sistema de salud, investigadores, y al colectivo de pacientes y familiares un mayor nivel de conocimiento acerca del número y distribución geográfica de las personas afectadas por ER en España. Se persigue así fomentar la investigación y aumentar la visibilidad de estas enfermedades, y favorecer la toma de decisiones para una adecuada planificación sanitaria y una correcta distribución de recursos.
El Registro de Pacientes de Enfermedades Raras tiene dos vías principales de entrada de información (casos): 1) a partir de la inclusión directa del paciente por parte del propio afectado o de un familiar o representante en https://registroraras.isciii.es/ y, 2) mediante los profesionales que incluyan la información de sus bases de datos (ya sean investigadores o sociedades médicas).

El registro se sustenta desde el punto de vista legal en la orden publicada en el B.O.E de junio de 2005, (ORDEN SCO/1730/2005, DE 31 DE MAYO), donde se establecieron los criterios de creación y funcionamiento, el lugar dónde debe estar depositada la custodia legal y la responsabilidad del mismo, y sobre su mantenimiento y ulterior desarrollo. Al mismo tiempo, este registro ha sido declarado de carácter oficial ante la Agencia Nacional de Protección de Datos, en cumplimiento de la normativa vigente relativa a la protección de datos personales con el número 2060180217.
Orientado a personas afectadas y sus familias:
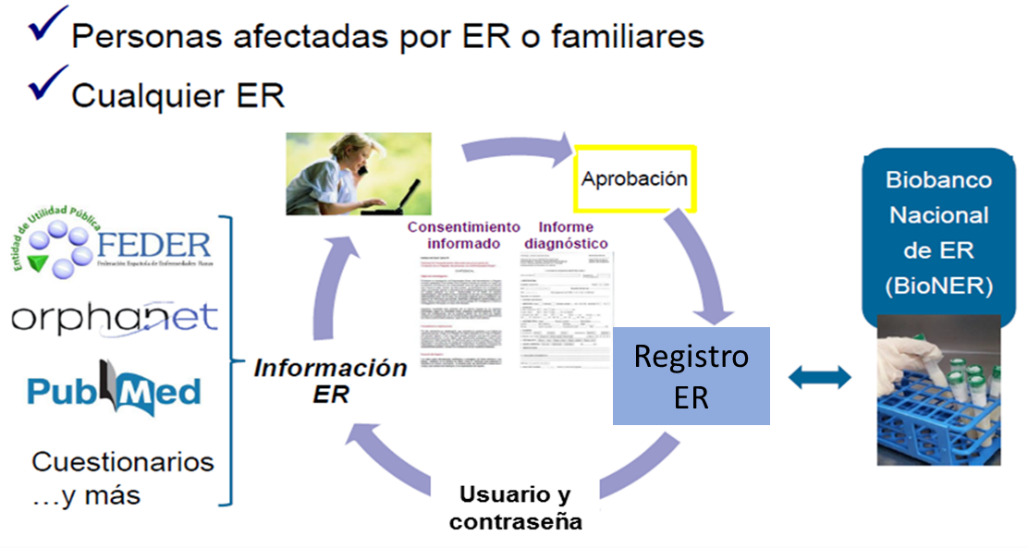
Cualquier persona afectada por ER, o familiar, puede inscribirse de forma voluntaria en el Registro de Pacientes de Enfermedades Raras.
Se ofrece a los propios pacientes o tutores (en caso de niños y personas incapacitadas) la oportunidad de inscribirse en este registro a través de la página web https://registroraras.isciii.es/. Una vez validada la solicitud, se proporciona un usuario y contraseña para que la persona inscrita pueda acceder al registro, consultar información sobre su enfermedad y participar en estudios mediante cuestionarios on-line sobre: uso de medicamentos, calidad de vida, análisis de la dependencia, recursos sanitarios, etc. Además, se ofrece la posibilidad de donar muestras biológicas, por su conexión con el Biobanco Nacional de Enfermedades Raras (BioNER).
Orientado a profesionales:
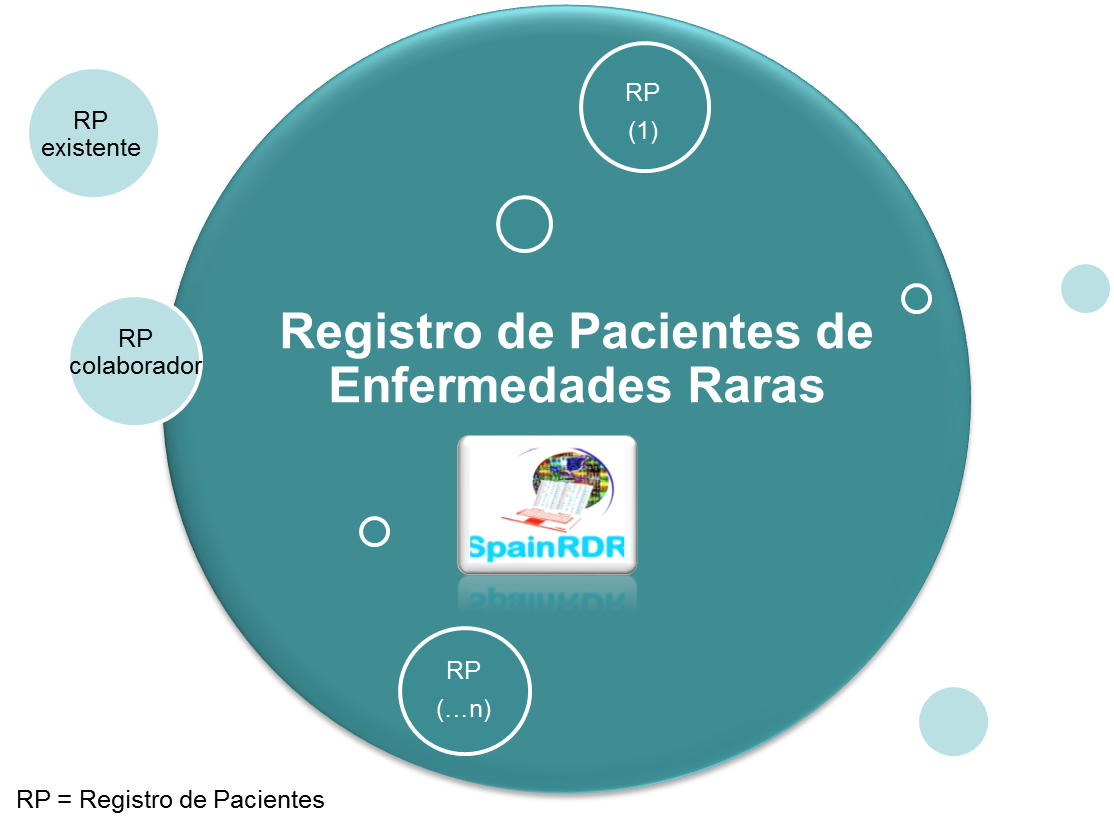
Los profesionales con experiencia en alguna enfermedad rara, con registros de pacientes ya existentes o con interés en desarrollar un nuevo registro, también pueden colaborar con el Registro de Pacientes de Enfermedades Raras y unificar esfuerzos.
Los registros de pacientes que colaboran mantienen su identidad, autonomía y gestión de datos y, al tiempo que se benefician de formar parte del Registro de Enfermedades Raras, se favorece la investigación, optimizan los recursos y respetan los derechos de los ciudadanos.
La incorporación de registros de pacientes a una red de investigación conlleva VENTAJAS como la reducción de costes, promoción, difusión y menor fragmentación del número de casos.
El Registro de Pacientes de Enfermedades Raras del ISCIII surge de la red de registros SpainRDR ofreciendo posibilidades de colaboración, sin menoscabo de la identidad o autonomía de cada registro.
Procedimiento de colaboración e incorporación de registros de pacientes:
- Con cada Sociedad o Grupo de investigación se firma un Convenio de colaboración con el Instituto de Investigación de Enfermedades Raras (IIER), Instituto de Salud Carlos III
- El compromiso de los profesionales participantes se manifiesta en un Acuerdo de Consorcio
- Se define el Modelo de datos en colaboración con los responsables, manteniendo la interoperabilidad entre registros de pacientes
- Se facilita el Consentimiento informado ya evaluado y aceptado por el Comité de Ética del IIER
- El Registro de Pacientes de ER está declarado en la Agencia Española de Protección de Datos, por lo que cualquier registro que se integre en él no precisaría una declaración propia
- Se facilita el Documento de seguridad del Registro de Pacientes de ER para mantener la confidencialidad
- Autorización de Acceso al registro mediante usuario y contraseña. Existen diferentes permisos de forma que cada grupo tendrá únicamente acceso a la información de los pacientes de su registro.
Si desea iniciar una colaboración, por favor escriba a: registro.raras@isciii.es
Resultados de investigación
La unidad de Terapia Génica es un grupo de investigación que, mediante el uso de modelos murinos y celulares, así como de terapias avanzadas, trabaja en: (i) la generación de modelos celulares y animales de enfermedades raras; (ii) el estudio de los mecanismos subyacentes al desarrollo y progresión de enfermedades humanas, y (iii) la búsqueda de nuevas aproximaciones terapéuticas para su tratamiento. Hasta la fecha, la unidad se ha centrado en tres tipos de enfermedades raras: la distrofia muscular congénita asociada a LMNA, los tumores ováricos de células de la granulosa y la leucoencefalopatía agresiva de aparición temprana asociada a KARS1.
El grupo inició su actividad científica en 2016 bajo la dirección del Dr. Pérez de Castro. Desde entonces, ha establecido contratos de colaboración con fundaciones de enfermedades raras con sede en España, Estados Unidos y Bélgica (Fundación Andrés Marcio, L-CMD Research Foundation, Cure CMD, CureKARS), y ha obtenido financiación procedente de convocatorias competitivas nacionales e internacionales.
Hasta la fecha, las principales contribuciones del grupo pueden resumirse del siguiente modo:
1. Caracterización de TRMT61B como nuevo biomarcador y diana terapéutica en cánceres altamente aneuploides (Martín et al., Cell Death and Differentiation, 2022, 30(1): 37-53 (https://doi.org/10.1038/s41418-022-01044-6).
2. Estudio del potencial de la tecnología CRISPR como estrategia terapéutica frente a los tumores de células de la granulosa, causalmente asociados a la mutación FOXL2-C134W (Amarilla-Quintana et al., Molecular Oncology 2025, 19: 1092-1116 (https://doi.org/10.1002/1878-0261.13799).
3. Generación y estudio de una colección de mioblastos murinos, generados mediante CRISPR, portadores de distintas mutaciones en el gen Lmna (Gómez-Domínguez et al., Cells 2020, 9, 1286 (https://doi.org/10.3390/cells9051286).
4. Generación de un modelo de Drosophila melanogaster para la expresión de LamCR264W, que recapitula el fenotipo muscular esquelético de la L-CMD (resultados no publicados).
5. Generación de un modelo murino LmnaR249W (manuscrito en preparación), que reproduce los fenotipos cardíacos observados en la distrofia muscular humana L-CMD. Este modelo ya ha sido utilizado para evaluar el potencial de diferentes estrategias terapéuticas.
6. Reversión de características asociadas a la enfermedad mediante la integración de un minigén LMNA de tipo salvaje, utilizando la tecnología HITI, en mioblastos humanos LMNA p.R249W y en ratones LmnaR249W/R249W (Epifano et al., Human Gene Therapy, 30(11): A160-A160, 2019.).
7. Eliminación específica, mediada por CRISPR, de la mutación LMNA c.745C>T, p.R249W en fibroblastos murinos y en ratones LmnaR249W (Gómez-Domínguez et al., 2025, bioRxiv 2025.02.13.638060; doi: https://doi.org/10.1101/2025.02.13.638060; (Molecular Therapy Advances; in press).
8. Estudio del potencial terapéutico del inhibidor de p38 ARRY-797 tanto en mioblastos humanos como en modelos animales (mosca LamCR264W y ratón LmnaR249W) (Epifano et al., 2023, J Neuromuscul Dis. 2023;10(s2):S47. doi: 10.3233/JND-239001).
9. Uso de editores ABE para la corrección de la mutación LMNA c.745C>T en células humanas y murinas. Ensayos de prueba de concepto para la futura aplicación de estas aproximaciones CRISPR 2.0 en L-CMD (Santafé et al., 2026, manuscript in preparation).
10. Generación y caracterización de controles isogénicos de tipo salvaje a partir de iPSCs de L-CMD editadas mediante editores ABE (trabajo en curso).