Desde el ISCIII mostramos nuestra solidaridad con todas las personas afectadas por el desastre de la DANA
Todo nuestro apoyo en estos momentos tan difíciles
Actualidad

Tecnologías de vanguardia para impulsar la identificación de enfermedades raras sin diagnóstico
El Instituto de Salud Carlos III (ISCIII), a través de su Instituto de Investigación de Enfermedades Raras (IIER), lleva años desarrollando un programa para mejorar el diagnóstico de patologías poco comunes especialmente difíciles de identificar. El Programa SpainUDP, creado en 2013, coordina la investigación y análisis de casos clínicos complejos para alcanzar un diagnóstico que es fundamental para superar barreras clínicas, sanitarias y sociales. El Día Mundial de las Personas Sin Diagnóstico, que se conmemora cada 29 de abril y que complementa el Día Mundial de las Enfermedades Raras (28 de febrero), es una oportunidad para visibilizar la necesidad de seguir impulsando la investigación para mejorar la identificación de patologías poco comunes difíciles de catalogar. Según explica Eva Bermejo, directora del IIER-ISCIII, "muchas personas afectadas, y sus familiares, esperan en ocasiones años e incluso décadas, hasta que la ciencia puede identificar la enfermedad que explique su condición". Según añade, la ausencia de diagnóstico dificulta el acceso a tratamientos adecuados, empeora la calidad de vida y supone una importante barrera sociosanitaria. Desde su nacimiento hace 13 años, el Programa SpainUDP -coordinado por las investigadoras Beatriz Martínez y Estrella López, junto con Eva Bermejo- ha recibido 647 propuestas de casos clínicos complejos para, en coordinación con los especialistas clínicos, tratar de acelerar un diagnóstico y facilitar la calidad de vida de las personas afectadas. Más de la mitad de las propuestas recibidas (373, casi un 58% del total) han sido aceptadas al cumplir los requisitos para su estudio y, de este total, más del 60% (227 casos) han sido ya completamente evaluadas (el resto están pendientes de nuevas pruebas o información adicional). De los casos analizados, que incluyen casos pediátricos y adultos, casi la mitad (108) han logrado finalmente un diagnóstico genético. SpainUDP ha diagnosticado el 52,5% de los casos pediátricos. Estos resultados han sido posibles gracias a la amplia red de colaboraciones nacionales e internacionales. Entre las colaboraciones nacionales destaca la red de clínicos directamente implicados en la atención a estos pacientes, ya que actúan como apoyo esencial para SpainUDP desde el tejido asistencial del Sistema Nacional de Salud. En el caso internacional, el partenariado europeo ERDERA ha comenzado este año un proceso de reanálisis sistemático de casos sin diagnóstico por toda Europa, que incluye pacientes procedentes del Programa SpainUDP. Esta labor de estudio permite reevaluar datos genéticos a la luz de nuevos conocimientos y herramientas tecnológicas, lo que permite aumentar las posibilidades diagnósticas. En este sentido, el IIER-ISCIII ha incorporado en los últimos años el uso de tecnologías de vanguardia para el análisis clínico y genético. Entre las incorporaciones más recientes destacan el mapeo óptico del genoma (OGM), la secuenciación del genoma mediante lecturas largas (long-read sequencing) y el estudio específico de genes RNU, recientemente identificados como una de las causas más frecuentes de síndromes del neurodesarrollo. Estos avances han permitido alcanzar diversos diagnósticos en casos no resueltos, entre ellos el diagnóstico del primer caso recibido en SpainUDP, en 2013. De izquierda a derecha: María José Barrero, Victoria Moneo, Esther Hernández, Marta Fernández, Sheila Ramos, Sergio Casas, Eva Bermejo, Estrella López, Beatriz Martínez, Raúl Contreras, Gema Gómez y Beatriz Baladrón, del IIER e implicados en el Progrma SpainUDP. En la imagen no aparece Lidia Mirela, que también forma parte del proyecto. En esta labor de impulso diagnóstico, el Programa SpainUDP integra diferentes estrategias para evaluar, mediante pruebas funcionales, el papel de nuevos genes que puedan ser causantes de enfermedad, pero que son actualmente desconocidos. Para ello, en la unidad de Modelos y Mecanismos liderada por Maria José Barrero, que también se integra en SpainUDP, se llevan a cabo iniciativas como el desarrollo en laboratorio de nuevos modelos celulares in vitro y la generación de modelos de organoides, mini-órganos artificiales que imitan el funcionamiento de órganos reales, sobre los que se pueden realizar las pruebas más adecuadas para cada caso. También en la Unidad de Modelos de Enfermedad en Drosophila, liderada por Sergio Casas, se estudian variantes genómicas y su funcionalidad en avatares creados en dicho organismo. De esta manera se mejora el estudio de la alteración de genes específicos como causantes de nuevos síndromes, por ejemplo en enfermedades del neurodesarrollo. Las coordinadoras del Programa SpainUDP en el IIER-ISCIII explican que este tipo de avances "pone de manifiesto que, incluso tras años de incertidumbre, la investigación y la innovación científica, y la revisión permanente con nuevas técnicas, de los casos que siguen sin identificar, pueden abrir nuevas vías para lograr un diagnóstico final. Para muchas personas la respuesta científica puede tardar, pero la investigación permite nuevos conocimientos que acercan el final de esa odisea por el desierto que, para algunas personas, puede suponer la búsqueda de diagnóstico para su enfermedad".
Saber más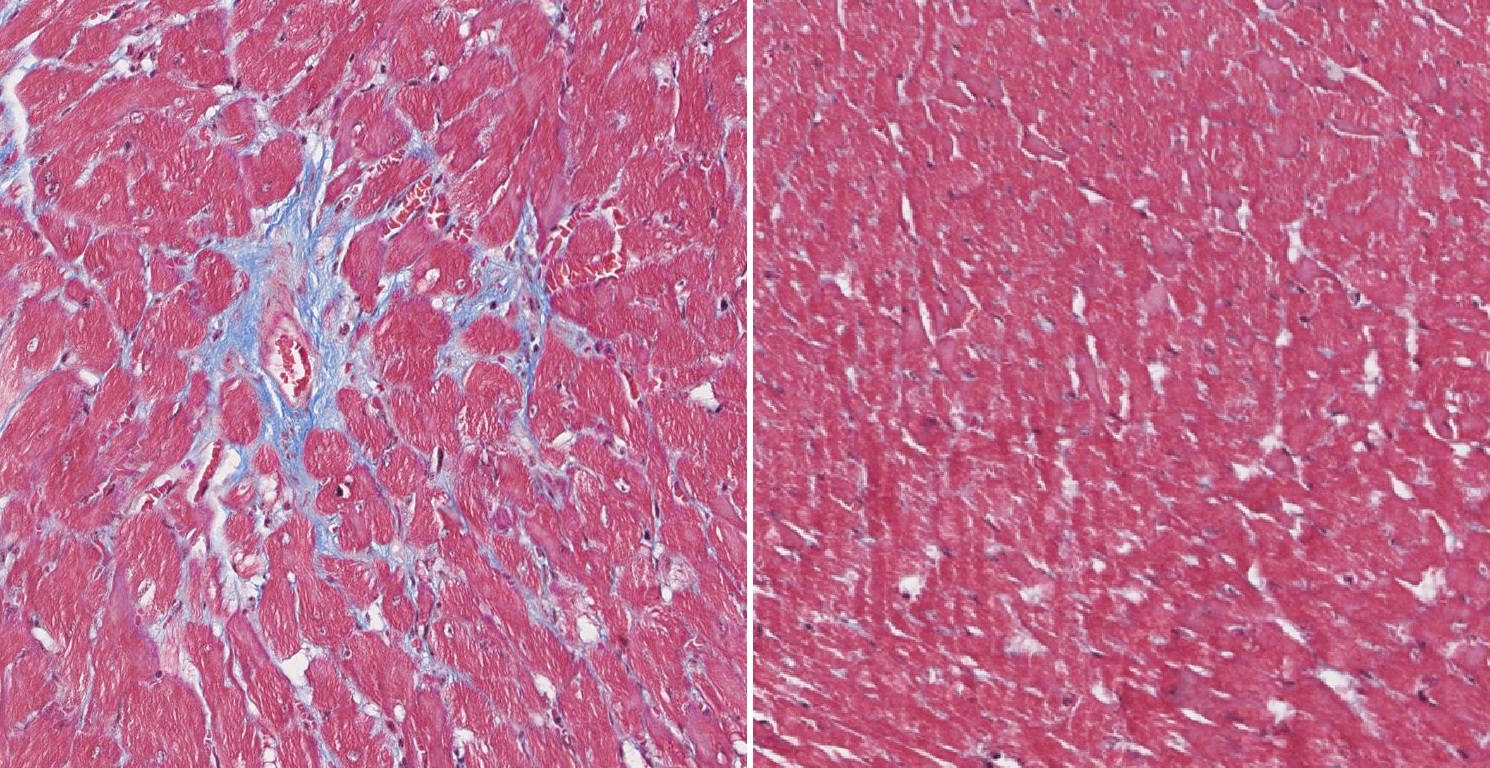
Primeros avances hacia una terapia génica con CRISPR para una enfermedad rara muscular sin cura
Una investigación del Instituto de Salus Carlos III (ISCIII) ha utilizado la herramienta de edición genética CRISPR para explorar un posible tratamiento para una enfermedad muscular muy poco común y sin cura, la distrofia muscular congénita asociada al gen LMNA (abreviada como L-CMD). El estudio, liderado por un equipo del Instituto de Investigación de Enfermedades Raras (IIER), se ha publicado en la revista Molecular Therapy Advances. Los resultados de este trabajo, llevado a cabo en modelos celulares y animales, sugieren un aumento de la supervivencia en esta patología sin cura, y representan la primera validación terapéutica de una estrategia de edición génica mediada por CRISPR-Cas9 para tratar la L-CMD. La distrofia muscular congénita asociada al gen LMNA es un trastorno genético raro, actualmente incurable, que se caracteriza por debilidad muscular de aparición temprana, problemas cardiacos como la miocardiopatía dilatada e insuficiencia respiratoria. Se trata de una patología monogénica, es decir, causada por mutaciones en un solo gen. La edición genética CRISPR, especialmente prometedora para tratar este tipo de patologías, se basa en un mecanismo de ‘tijeras moleculares’ para modificar el ADN con precisión; permite cortar, eliminar o reemplazar secuencias específicas del genoma, lo que abre grandes vías para tratar enfermedades genéticas. El equipo del ISCIII, liderado por el doctor Ignacio Pérez de Castro, ha evaluado el potencial de CRISPR para eliminar la mutación más frecuentemente asociada a esta enfermedad, Lmna c.745C>T, p.R249W, utilizando para ello una guía específica, denominada sg745T. En modelos celulares, portadores de la citada alteración genética, han confirmado que el complejo Cas9/sg745T muestra una actividad específica hacia este alelo mutado dependiente de la dosis utilizada. Tras los resultados in vitro, análisis en un modelo de ratón confirmaron el potencial de esta estrategia gracias a la administración de la terapia usando virus adenoasociados en ratones portadores de la mutación causante de la enfermedad. La terapia aplicada a estos avatares murinos de pacientes humanos mejoró de manera significativa la patología cardiaca asociada a la enfermedad, lo que permitió incrementar la supervivencia media de los animales en más de un 20%. Este resultado adquiere especial relevancia si se considera que menos del 10% de los cardiomiocitos fueron editados por la maquinaria CRISPR en los animales tratados. De izda a dcha: Mercedes Dessy (Investigadora postdoctoral), Mónica Ferreiro (estudiante de grado, TFG), Mario Santafé (estudiante de doctorado), Iván Hernández (técnico especializado), Maria Luisa Martínez (técnica superior especializada), Ignacio Pérez de Castro (Jefe del grupo de Terapia Génica del IIER-ISCIII, investigador científico), Déborah Gómez (investigadora postdoctoral), Paula Esteban (estudiante de doctorado) y Alfredo Corral (estudiante de grado, TFG). El doctor Pérez de Castro explica que este estudio supone un primer paso hacia el desarrollo de una terapia capaz de aumentar la supervivencia y, potencialmente, curar la L-CMD. Asimismo, refuerza el potencial de la terapia génica basada en CRISPR para el abordaje de enfermedades raras como las laminopatías (enlace a esta noticia previa). "Aunque la eficiencia de edición obtenida hasta ahora es limitada, los resultados son prometedores y han superado nuestras expectativas. Ya estamos trabajando para superar estas barreras mediante el uso de editores evolucionados y la optimización de los sistemas de entrega de los complejos CRISPR. Nuestro objetivo es desarrollar una terapia de precisión que beneficie al mayor número posible de pacientes con esta enfermedad rara y que, además, sirva como plataforma para futuros tratamientos personalizados dirigidos a portadores de otras mutaciones en el gen LMNA o a pacientes con distrofias musculares causadas por mutaciones puntuales en otros genes". • Referencia del artículo: CRISPR-mediated targeting of the LMNA c.745C>T mutation enhances survival and cardiac function in congenital muscular dystrophy. Gómez-Domínguez, Déborah et al. Molecular Therapy Advances, Volume 34, Issue 1, 201653. https://www.cell.com/molecular-therapy-family/advances/fulltext/S3117-387X(25)00003-5. Vídeo divulgativo sobre la investigación y sus principales resultados. Youtube ISCIII.
Saber más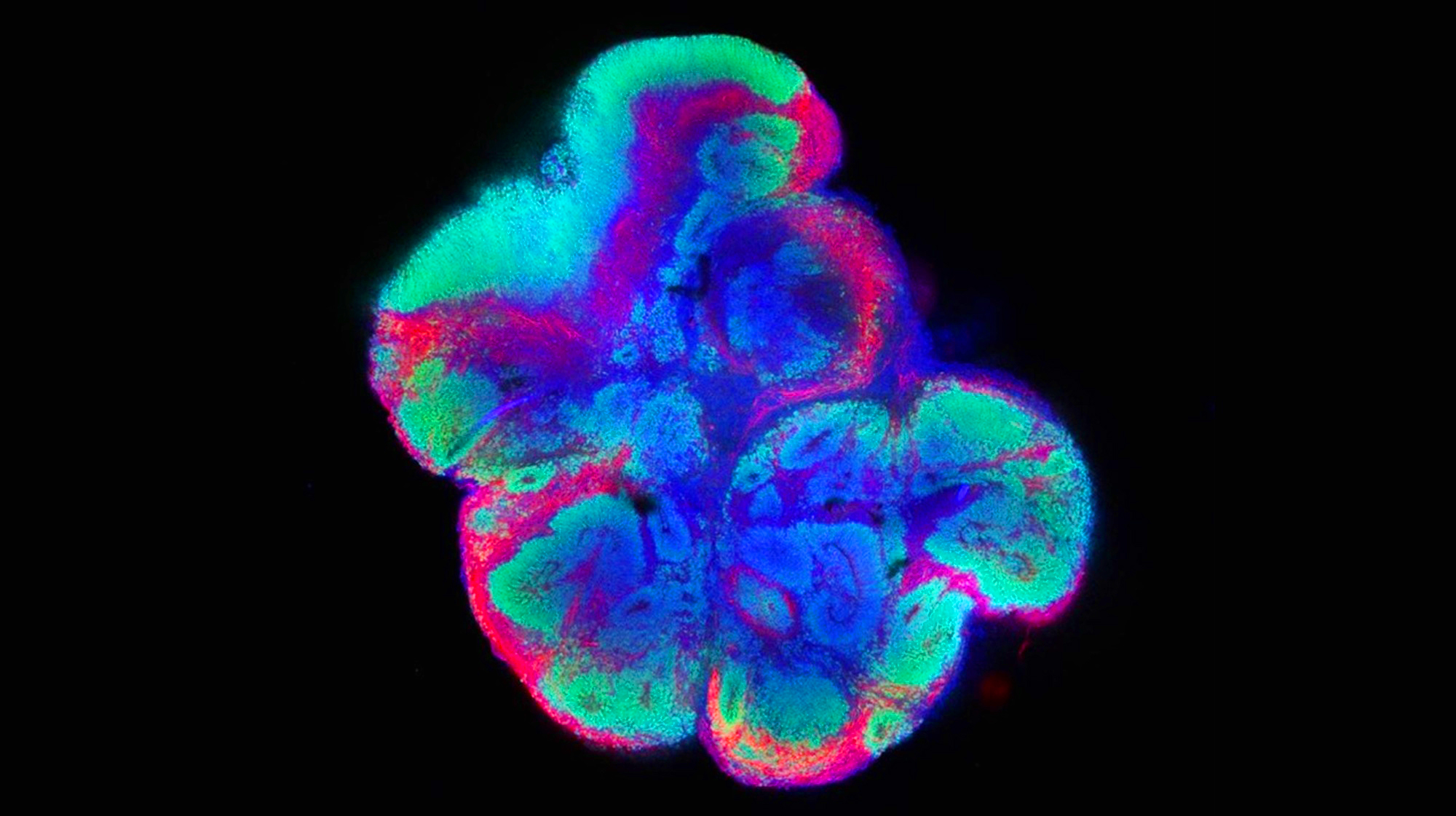
El ISCIII comienza con apoyo de FEDER un proyecto pionero para estudiar el ‘mapa del cerebro’ en el síndrome de Kleefstra
Un equipo del Instituto de Salud Carlos III (ISCIII) va a llevar a cabo un innovador estudio que permitirá trazar el ‘mapa del cerebro’ en el síndrome de Kleefstra, una enfermedad rara de origen genético que afecta al desarrollo neurológico. Esta investigación está impulsada por una ayuda concedida al Instituto de Investigación de Enfermedades Raras (IIER) del ISCIII por la Federación Española de Enfermedades Raras (FEDER), en su IX Convocatoria de Ayudas a la Investigación de la Fundación FEDER. El proyecto, que se va a realizar en colaboración la Asociación de pacientes Kleefstra España, tiene como objetivo comprender mejor cómo se organiza y funciona el cerebro en las personas con esta alteración, identificando los circuitos neuronales implicados en sus principales manifestaciones clínicas, como las dificultades cognitivas, del lenguaje y del comportamiento. Mediante el uso de tecnologías de vanguardia, entre las que se incluyen modelos celulares derivados de pacientes, generación de organoides cerebrales y análisis avanzados de transcriptómica espacial, los investigadores e investigadoras del IIER-ISCIII esperan generar conocimiento que siente las bases de futuros tratamientos personalizados. Este proyecto reafirma el compromiso del ISCIII y de FEDER de apoyo a la investigación traslacional en enfermedades raras, impulsando estudios que acerquen soluciones a los pacientes y sus familias. La citada convocatoria de ayudas de FEDER incluye como condición indispensable para las solicitudes que los proyectos científicos se presenten de la mano de una de las asociaciones de pacientes miembro de FEDER, que también ha de presentar su expresión de interés por el proyecto. El ISCIII tiene una cercana relación de colaboración con FEDER, asociación con la que mantiene diversas líneas de colaboración, muestra del compromiso del Instituto con los pacientes y familiares con enfermedades raras. "Este estudio nos permitirá obtener una visión sin precedentes del cerebro en el síndrome de Kleefstra, y abre la puerta a la posible identificación de dianas terapéuticas que podrían mejorar la calidad de vida de las personas afectadas", concluye la doctora María José Barrero, del IIER-ISCIII e investigadora principal del proyecto.
Saber másAnota estas fechas
17 oct
17 sep
Empleo
IERPY 122-25-1-2-M3 (IND)
Inicio de plazo: 28/04/2026
Fin de plazo: 12/05/2026
Clase de personal: Laboral
Procedimiento / Modalidad: Indefinido (Art. 23 bis LCTI)
IERPY 122/25-BIS-M3-1 INDEFINIDO; INTPY 362/22- M3-4 y 5 INDEFINIDO
Inicio de plazo: 03/12/2025
Fin de plazo: 17/12/2025
Clase de personal: Laboral
Procedimiento / Modalidad: Indefinido (Art. 23 bis LCTI)
COOPERA 3M3y2M2 (IND)
Inicio de plazo: 19/11/2025
Fin de plazo: 02/12/2025
Clase de personal: Laboral
Procedimiento / Modalidad: Indefinido (Art. 23 bis LCTI)



