Unidad de Investigación en Modelos y Mecanismos

Líneas de investigación
Content with Investigacion .
Terapia Génica
Nuestro grupo está centrado en (i) la investigación de los mecanismos subyacentes a distintos tipos de tumores huérfanos y enfermedades raras y (ii) la búsqueda de nuevas estrategias terapéuticas para combatir las enfermedades raras.
Nuestras líneas de investigación están actualmente enfocadas en los tumores de la granulosa ovárica asociados a FOXL2, la leucoencefalopatía agresiva precoz relacionada con KARS1 y en las distrofias musculares congénitas asociadas a LMNA. En todos los casos el editado génico mediado por CRISPR es la aproximación terapéutica mayormente seleccionada.
Contamos con la siguiente financiación:
- Evolución de estrategias terapéuticas basadas en CRISPR/Cas con potencial para el tratamiento de la distrofia muscular congénita asociada a LMNA (PI23CIII/00041). Acción Estratégica en Salud Intramural ISCIII 2023. IP: Ignacio Pérez de Castro. 2025-27. 138000€.
- La vía de los glucocorticoides en la distrofia muscular congénita relacionada con LMNA: Descifrando mecanismos y probando estrategias terapéuticas (PID2023-147678OB-I00). Proyectos Generación de Conocimiento AEI 2023. IP: Ignacio Pérez de Castro. 2025-27. 275000€.
- Investigating the potential of Replacement Gene Therapy for Early-Onset Progressive Leukoencephalopathy using iPSCs and a Kras1 knock-in mouse model. Cure KARS Laia Foundation. IP: Ignacio Pérez de Castro. 2025-28. 250000€.
- Distrofias congénitas asociadas a LMNA. LCMD-Research Foundation. IP: Ignacio Pérez de Castro. 2026-27. 43000€.
Publicaciones destacadas
CREBBP/EP300 bromodomain inhibition affects the proliferation of AR positive breast cancer cell lines. (2019) Molecular Cancer Research. 17 (3): 720–730.
Garcia-Carpizo V, Ruiz-Llorente S, Sarmentero J, Gonzalez-Corpas A and Barrero MJ.
DOICREBBP/EP300 bromodomains are critical to sustain the GATA1/MYC regulatory axis in proliferation. (2018) Epigenetics and Chromatin 11:30.
Garcia-Carpizo V, Ruiz-Llorente S, Sarmentero J, Graña O, Pisano DG and Barrero MJ.
DOINSD2 contributes to oncogenic RAS-driven transcription in lung cancer cells through long-range epigenetic activation. (2016) Scientific Reports. 6:32952.
Garcia-Carpizo V, Sarmentero J, Han B, Graña O, Ruiz-Llorente S, Pisano DG, Serrano M, Brooks HB, Campbell RM, Barrero MJ.
DOISETD7 Regulates the Differentiation of Human Embryonic Stem Cells. (2016) PLoS One. 11(2): e0149502.
Castaño J, Morera C, Sesé B, Boue S, Bonet-Costa C, Martí M, Roque A, Jordan A, Barrero MJ.
DOIMacro Histone Variants are Critical for the Differentiation of Human Pluripotent Cells. (2013) Journal of Biological Chemistry. 288(22):16110-6.
Barrero MJ, Sese B, Marti M and Izpisua Belmonte JC.
DOIMacro Histone Variants Preserve Cell Identity by Preventing the Gain of H3K4me2 during Reprogramming to Pluripotency. (2013) Cell Reports 3, 1005–1011.
Barrero MJ, Sese B, Kuebler B, Bilic J, Boue S, Martí M, Belmonte JC.
DOIMediator-regulated transcription through the +1 nucleosome. (2012) Molecular Cell. 48(6):837-48.
Nock A, Ascano JA, Barrero MJ and Malik S.
DOIAlu-repeat mediated regulation of DIEXF expression in cell differentiation and cancer. (2020) Epigenetics 15(6-7):765-779.
Martín B, Pappa S. Díez-Villanueva A, Mallona I, Custodio J, Barrero MJ, Peinado MA, Jordà M.
DOIDNA Methylomes Reveal Biological Networks Involved in Human Eye Development, Functions and Associated Disorders. Sci Rep. (2017) 7(1):11762.
Berdasco M, Gómez A, Rubio MJ, Català-Mora J, Zanón-Moreno V, Lopez M, Hernández C, Yoshida S, Nakama T, Ishikawa K, Ishibashi T, Boubekeur AM, Louhibi L, Pujana MA, Sayols S, Setien F, Corella D, de Torres C, Parareda A, Mora J, Zhao L, Zhang K, Lleonart ME, Alonso J, Simó R, Caminal JM, Esteller M.
PUBMED DOIEWS-FLI1-mediated suppression of the RAS-antagonist Sprouty 1 (SPRY1) confers aggressiveness to Ewing sarcoma. Oncogene (2017) 36(6):766-776.
Cidre-Aranaz F, Grünewald TG, Surdez D, García-García L, Carlos Lázaro J, Kirchner T, González-González L, Sastre A, García-Miguel P, López-Pérez SE, Monzón S, Delattre O, Alonso J.
PUBMED DOIFamilial retinoblastoma due to intronic LINE-1 insertion causes aberrant and non-canonical mRNA splicing of the RB1 gene. J Hum Genet (2016) 61(5):463-6.
Rodríguez-Martín C., Cidre-Aranaz F., Fernández-Teijeiro A., Gómez-Mariano G., de la Vega L., Ramos P., Zaballos A., Monzón S., Alonso J.
PUBMED DOIChimeric EWSR1-FLI1 regulates the Ewing sarcoma susceptibility gene EGR2 via a GGAA-microsatellite. Nature Genetics (2015) 47(9):1073-8.
Grünewald T.G.P., Bernard V., Gilardi-Hebenstreit P., Raynal V., Surdez D., Aynaud M.M., Mirabeau O., Cidre-Aranaz F., Tirode F., Zaidi S., Perot G., Jonker A.H., Lucchesi C., Le Deley M.C., Oberlin O., Marec-Bérard P., Véron A.S., Reynaud S., Lapouble E., Boeva V., Frio T.R, Alonso J., Bhatia S., Pierron G., Cancel-Tassin G., Cussenot O., Cox D.G., Morton L.M., Machiela M., Chanock S.J., Charnay P., Delattre O.
PUBMED DOISelective inhibition of plasma membrane calcium ATPase4 improves angiogénesis and vascular reperfusion. 2017. J. Mol. Cell. Cardiol. 109: 38-47.
Kurusamy S., López-Maderuelo D., Little R., Cadagan D., Savage A.M., Ihugba J.C., Baggott RR, Rowther FB., Martínez-Martínez S, Gómez-del Arco P., Murcott C., Wang W., Nistal F.J., Oceandy D, Neyses L, Wilkinson R.N., Cartwright EJ, Redondo J.M. and A.L. Armesilla.
PUBMED DOIThe Chromatin Remodeling Complex Chd4/NuRD controls striated muscle identity and metabolic homeostasis. 2016. Cell Metabolism. 23: 881-892.
Gómez-del Arco P*., Perdiguero E., Yunes-Leites P.S., Acín-Pérez R., Zeini M., García-Gómez A., Sreenivasan K., Jiménez-Alcázar M., Segalés J., López-Maderuelo D., Ornés B., Jiménez-Borreguero L.J., D´Amato G., Enshell-Seijffers D., Morgan B., Georgopoulos K., Islam AbuL B.M.M.K., Braun T., de la Pompa J.L., Kim J., Enriquez J.A., Ballestar E,, Muñoz-Cánoves P. and Redondo J.M*. *corresponding authors.
PUBMED DOISequential ligand-dependent Notch signaling activation regulates valve primordium formation and morphogenesis. 2016. Circulation Research. 118 (10): 1480-1497.
MacGrogan D., D´Amato G., Travisano S., Martinez-Poveda B., Luxán G., del Monte-Nieto G., Papoutsi T., Sbroggio M., Bou V., Gómez-del Arco P., Gómez M.J., Zhou B., Redondo J.M., Jiménez-Borreguero L.J., de la Pompa J.L.
PUBMED DOIPlasma membrane calcium ATPase isoform 4 inhibits vascular endothelial growth factor-mediated angiogenesis through interaction with calcineurin. 2014. Arterioscler. Thromb. Vasc. Biol. Volumen: 34: 2310-2320.
Baggott RR, Alfranca A, López-Maderuelo D, Mohamed TM, Escolano A, Oller J, Ornes BC, Kurusamy S, Rowther FB, Brown JE, Oceandy D, Cartwright EJ, Wang W, Gómez-del Arco P, Martínez-Martínez S., Neyses L, Redondo JM, Armesilla AL.
PUBMED DOIAlternative promoter usage at the Notch1 locus supports ligand-independent signaling in T cell development and leukemogenesis. 2010. Immunity. 33(5): 685-698.
Pablo Gómez-del Arco, Mariko Kashiwagi, Audrey F. Jackson, Taku Naito, Jiangwen Zhang, Feifei Liu, Barbara Kee, Marc Vooijs, Freddy Radtke, Juan Miguel Redondo and Katia Georgopoulos.
PUBMED DOIMAZ induces MYB expression during the exit from quiescence via the E2F site in the MYB promoter. 2017. Nucleic Acids Research. 45 (17): 9960-9975.
Alvaro-Blanco J., Urso K., Chiodo Y., Martín-Cortázar C., Kourani O., Gómez-del Arco P., Rodríguez-Martínez M., Calonge E., Alcamí J., Redondo JM., Iglesias T., and MR. Campanero.
PUBMED DOILiver organoids reproduce alpha-1 antitrypsin deficiency-related liver disease
Gómez-Mariano G, Matamala N, Martínez S, Justo I, Marcacuzco A, Jimenez C, Monzón S, Cuesta I, Garfia C, Martínez MT, Huch M, Pérez de Castro I, Posada M, Janciauskiene S, Martínez-Delgado B. Liver organoids reproduce alpha-1 antitrypsin deficiency-related liver disease. Hepatol Int. 2020 Jan;14(1):127-137.
PUBMED DOIToxic oil syndrome: healthrelated quality-of-life assessment using the SF-36 Health Survey. International Journal of Epidemiology, 51(2), 491–500.
DOI
Comprehensive reanalysis for CNVs in ES data from unsolved rare disease cases results in new diagnoses. NPJ Genom Med. 2024 Oct 26;9(1):49
Demidov G, Yaldiz B, Garcia-Pelaez J, de Boer E, Schuermans N, Van de Vondel L, Paramonov I, Johansson LF, Musacchia F, Benetti E, Bullich G, Sablauskas K, Beltran S, Gilissen C, Hoischen A, Ossowski S, de Voer R, Lohmann K, Oliveira C, Topf A, Vissers LELM; Solve-RD Consortium; Laurie S.
PUBMED DOIPushing the boundaries of rare disease diagnostics with the help of the first Undiagnosed Hackathon. Nat Genet. 2024 Nov;56(11):2287-2294
Delgado-Vega AM, Cederroth H, Taylan F, Ekholm K, Ek M, Thonberg H, Jemt A, Nilsson D, Eisfeldt J, Bilgrav Saether K, Höijer I, Akgun-Dogan O, Asano Y, Barakat TS, Batkovskyte D, Baynam G, Bodamer O, Chetruengchai W, Corcoran P, Couse M, Danis D, Demidov G, Dohi E, Erhardsson M, Fernandez-Luna L, Fujiwara T, Garg N, Giugliani R, Gonzaga-Jauregui C, Grigelioniene G, Groza T, Gunnarsson C, Hammarsjö A, Hammond CK, Hatirnaz Ng Ö, Hesketh S, Hettiarachchi D, Johansson Soller M, Kirmani UA, Kjellberg M, Kvarnung M, Kvlividze O, Lagerstedt-Robinson K, Lasko P, Lassmann T, Lau LYS, Laurie S, Lim WK, Liu Z, Lysenkova Wiklander M, Makay P, Maiga AB, Maya-González C, Meyn MS, Neethiraj R, Nigro V, Nordgren F, Nordlund J, Orrsjö S, Ottosson J, Ozbek U, Özdemir Ö, Partin C, Pearce DA, Peck R, Pedersen A, Pettersson M, Pongpanich M, Posada de la Paz M, Ramani A, Romero JA, Romero VI, Rosenquist R, Saw AM, Spencer M, Stattin EL, Srichomthong C, Tapia-Paez I, Taruscio D, Taylor JP, Tkemaladze T, Tully I, Tümer Z, van Zelst-Stams WAG, Verloes A, Västerviga E, Wang S, Yang R, Yamamoto S, Yépez VA, Zhang Q, Shotelersuk V, Wiafe SA, Alanay Y, Botto LD, Kirmani S, Lumaka A, Palmer EE, Puri RD, Wirta V, Lindstrand A, Buske OJ, Cederroth M, Nordgren A.
PUBMED DOICIBERER: Spanish national network for research on rare diseases: A highly productive collaborative initiative. Clin Genet. 2022 May 10; 1(5-6):481-493
Luque J, Mendes I, Gómez B, Morte B, López de Heredia M, Herreras E, Corrochano V, Bueren J, Gallano P, Artuch R, Fillat C, Pérez-Jurado LA, Montoliu L, Carracedo Á, Millán JM, Webb SM, Palau F; CIBERER Network; Lapunzina P..
PUBMED DOIPrevalence of dystrophic epidermolysis bullosa in Spain: a population-based study using the 3-source capture-recapture method. Evidence of a need for improvement in care. Actas Dermosifiliogr. 2013 Dec;104(10):890-6
Hernandez-Martín A, Aranegui B, Escámez MJ, de Lucas R, Vicente A, Rodríguez-Díaz E, Bernabeu-Wittel J, Gonzalez-Hermosa R, García-Patos V, Ginarte M, Mascaró JM Jr, Corredera C, Baselga E, Santiago JL, Chaves A, Román C, Evole M, Martin-Santiago A, Torrelo A, Del Río M, Feito M, Gonzalez-Enseñat MA, Romero G, Morcillo-Makow E, Abaitua I, García-Doval I.
PUBMED DOIOverview of existing initiatives to develop and improve access and data sharing in rare disease registries and biobanks worldwide. Expert Opinion on Orphan Drugs, 4(7), 729–739
López-Martín E, Thompson R, Gainotti S, Wang CM, Rubinstein Y, Taruscio D, Monaco L, Lochmüller H, Alonso-Ferreira V, Posada de la Paz M.
DOIJiménez-García L, Higueras MÁ, Herranz S, Hernández-López M, Luque A, de Las Heras B, Hortelano S. A hispanolone-derived diterpenoid inhibits M2-Macrophage polarization in vitro via JAK/STAT and attenuates chitin induced inflammation in vivo. Biochem Pharmacol. 2018 Aug;154:373-383
Jiménez-García L, Higueras MÁ, Herranz S, Hernández-López M, Luque A, de Las Heras B, Hortelano S. A hispanolone-derived diterpenoid inhibits M2-Macrophage polarization in vitro via JAK/STAT and attenuates chitin induced inflammation in vivo. Biochem Pharmacol. 2018 Aug;154:373-383
PUBMED DOIJiménez-García L, Herranz S, Higueras MA, Luque A, Hortelano S. Tumor suppressor ARF regulates tissue microenvironment and tumor growth through modulation of macrophage polarization. Oncotarget. 2016 Oct 11;7(41):66835-66850.
Jiménez-García L, Herranz S, Higueras MA, Luque A, Hortelano S. Tumor suppressor ARF regulates tissue microenvironment and tumor growth through modulation of macrophage polarization. Oncotarget. 2016 Oct 11;7(41):66835-66850.
PUBMED DOIJiménez-García L, Través PG, López-Fontal R, Herranz S, Higueras MA, de Las Heras B, Hortelano S, Luque A. 8,9-Dehydrohispanolone-15,16-lactol diterpene prevents LPS-triggered inflammatory responses by inhibiting endothelial activation. Biochem J. 2016 Jul 15;473(14):2061-71.
Jiménez-García L, Través PG, López-Fontal R, Herranz S, Higueras MA, de Las Heras B, Hortelano S, Luque A. 8,9-Dehydrohispanolone-15,16-lactol diterpene prevents LPS-triggered inflammatory responses by inhibiting endothelial activation. Biochem J. 2016 Jul 15;473(14):2061-71.
PUBMED DOIGarcía-Quintans N, Prieto I, Sánchez-Ramos C, Luque A, Arza E, Olmos Y, Monsalve M. Regulation of endothelial dynamics by PGC-1α relies on ROS control of VEGF-A signaling. Free Radic Biol Med. 2016 Apr;93:41-51
García-Quintans N, Prieto I, Sánchez-Ramos C, Luque A, Arza E, Olmos Y, Monsalve M. Regulation of endothelial dynamics by PGC-1α relies on ROS control of VEGF-A signaling. Free Radic Biol Med. 2016 Apr;93:41-51
PUBMED DOIAbós B, Wang T, Castro R, Granja AG, Leal E, Havixbeck J, Luque A, Barreda DR, Secombes CJ, Tafalla C. Distinct Differentiation Programs Triggered by IL-6 and LPS in Teleost IgM(+) B Cells in The Absence of Germinal Centers. Sci Rep. 2016 Aug 2;6:30004
Abós B, Wang T, Castro R, Granja AG, Leal E, Havixbeck J, Luque A, Barreda DR, Secombes CJ, Tafalla C. Distinct Differentiation Programs Triggered by IL-6 and LPS in Teleost IgM(+) B Cells in The Absence of Germinal Centers. Sci Rep. 2016 Aug 2;6:30004
PUBMED DOIMaría Luisa Franco, Cristina Melero, Esther Sarasola, Alfonso Luque, María García-Barcina and Marçal Vilar. Mutations in TrkA Causing Congenital Insensitivity to Pain with Anhidrosis (CIPA) Induce Mutation-Dependent Misfolding, Aggregation and Cell Death. J Biol Chem. 2016 Aug 22. pii: jbc.M116.722587
María Luisa Franco, Cristina Melero, Esther Sarasola, Alfonso Luque, María García-Barcina and Marçal Vilar. Mutations in TrkA Causing Congenital Insensitivity to Pain with Anhidrosis (CIPA) Induce Mutation-Dependent Misfolding, Aggregation and Cell Death. J Biol Chem. 2016 Aug 22. pii: jbc.M116.722587
PUBMED DOIα-Hispanolol sensitizes hepatocellular carcinoma cells to TRAIL-induced apoptosis via death receptor up-regulation. Mota A, Jiménez-Garcia L, Herránz S, de Las Heras B, Hortelano S. Toxicol Appl Pharmacol. 2015 Aug 1;286(3):168-77.
α-Hispanolol sensitizes hepatocellular carcinoma cells to TRAIL-induced apoptosis via death receptor up-regulation. Mota A, Jiménez-Garcia L, Herránz S, de Las Heras B, Hortelano S. Toxicol Appl Pharmacol. 2015 Aug 1;286(3):168-77.
PUBMED DOICritical role of p38 MAPK in IL-4-induced alternative activation of peritoneal macrophages. Jiménez-Garcia L, Herránz S, Luque A, Hortelano S. Eur J Immunol. 2015 Jan;45(1):273-86
Critical role of p38 MAPK in IL-4-induced alternative activation of peritoneal macrophages. Jiménez-Garcia L, Herránz S, Luque A, Hortelano S. Eur J Immunol. 2015 Jan;45(1):273-86
PUBMED DOIIL10 released by a new inflammation-regulated lentiviral system efficiently attenuates zymosan-induced arthritis. Garaulet G, Alfranca A, Torrente M, Escolano A, López-Fontal R, Hortelano S, Redondo JM, Rodríguez A. Mol Ther. 2013 Jan;21(1):119-30.
IL10 released by a new inflammation-regulated lentiviral system efficiently attenuates zymosan-induced arthritis. Garaulet G, Alfranca A, Torrente M, Escolano A, López-Fontal R, Hortelano S, Redondo JM, Rodríguez A. Mol Ther. 2013 Jan;21(1):119-30.
PUBMED DOICritical role of the death receptor pathway in the antitumoral effects induced by hispanolone derivatives. Través PG, López-Fontal R, Cuadrado I, Luque A, Boscá L, de las Heras B, Hortelano S. Oncogene. 2013 Jan 10;32(2):259-68.
Critical role of the death receptor pathway in the antitumoral effects induced by hispanolone derivatives. Través PG, López-Fontal R, Cuadrado I, Luque A, Boscá L, de las Heras B, Hortelano S. Oncogene. 2013 Jan 10;32(2):259-68.
PUBMED DOILaura Hidalgo, Beatriz Somovilla-Crespo, Patricia Garcia-Rodriguez, Alvaro Morales Molina, Miguel Angel Rodriguez-Milla, Javier Garcia-Castro. Switchable CAR T cell strategy against osteosarcoma. Cancer Immunol Immunother. 2023 Aug;72(8):2623-2633.
Laura Hidalgo, Beatriz Somovilla-Crespo, Patricia Garcia-Rodriguez, Alvaro Morales Molina, Miguel Angel Rodriguez-Milla, Javier Garcia-Castro. Switchable CAR T cell strategy against osteosarcoma. Cancer Immunol Immunother. 2023 Aug;72(8):2623-2633.
PUBMED DOIAlvaro Morales-Molina, Miguel Ángel Rodriguez-Milla, Stefano Gambera, Teresa Cejalvo, Belén de Andrés, María-Luisa Gaspar, Javier García-Castro. Toll-like Receptor Signaling-deficient Cells Enhance Antitumor Activity of Cell-basedImmunotherapy by Increasing Tumor Homing. Cancer Res Commun. 2023 Mar 1;3(3):347-360.
Alvaro Morales-Molina, Miguel Ángel Rodriguez-Milla, Stefano Gambera, Teresa Cejalvo, Belén de Andrés, María-Luisa Gaspar, Javier García-Castro. Toll-like Receptor Signaling-deficient Cells Enhance Antitumor Activity of Cell-basedImmunotherapy by Increasing Tumor Homing. Cancer Res Commun. 2023 Mar 1;3(3):347-360.
PUBMED DOIAna Cloquell, Isidro Mateo, Stefano Gambera, Martí Pumarola, Ramón Alemany, Javier Garcia-Castro, Judith Perisé-Barrios. Systemic cellular viroimmunotherapy for canine high-grade gliomas. J Immunother Cancer. 2022 Dec;10(12): e005669.
Ana Cloquell, Isidro Mateo, Stefano Gambera, Martí Pumarola, Ramón Alemany, Javier Garcia-Castro, Judith Perisé-Barrios. Systemic cellular viroimmunotherapy for canine high-grade gliomas. J Immunother Cancer. 2022 Dec;10(12): e005669.
PUBMED DOIClara Martín-Carrasco, Pablo Delgado-Bonet, Beatriz Davinia Tomeo-Martín, Josep Pastor, Claudia de la Riva, Paula Palau-Concejo, Noemí del Castillo, Javier García-Castro, Ana Judith Perisé-Barrios. Safety and Efficacy of an Oncolytic Adenovirus as an Immunotherapy for Canine Cancer Patients. Vet Sci. 2022 Jul; 9(7): 327
Clara Martín-Carrasco, Pablo Delgado-Bonet, Beatriz Davinia Tomeo-Martín, Josep Pastor, Claudia de la Riva, Paula Palau-Concejo, Noemí del Castillo, Javier García-Castro, Ana Judith Perisé-Barrios. Safety and Efficacy of an Oncolytic Adenovirus as an Immunotherapy for Canine Cancer Patients. Vet Sci. 2022 Jul; 9(7): 327
PUBMED DOIMarion Rabé, Lucie Fonteneau, Lisa Oliver, Alvaro Morales-Molina, Camille Jubelin, Javier Garcia-Castro, Dominique Heymann, Catherine Gratas, François M. Vallette. Cellular Heterogeneity and Cooperativity in Glioma Persister Cells Under Temozolomide Treatment Frontiers in Cell and Developmental Biology. 2022, 10; 835273.
Marion Rabé, Lucie Fonteneau, Lisa Oliver, Alvaro Morales-Molina, Camille Jubelin, Javier Garcia-Castro, Dominique Heymann, Catherine Gratas, François M. Vallette. Cellular Heterogeneity and Cooperativity in Glioma Persister Cells Under Temozolomide Treatment Frontiers in Cell and Developmental Biology. 2022, 10; 835273.
PUBMED DOIAlvaro Morales-Molina, Stefano Gambera, Angela Leo, Javier García-Castro Combination immunotherapy using G-CSF and oncolytic virotherapy reduces tumor growth in osteosarcoma. J Immunother Cancer. 2021 Mar;9(3): e001703.
Alvaro Morales-Molina, Stefano Gambera, Angela Leo, Javier García-Castro Combination immunotherapy using G-CSF and oncolytic virotherapy reduces tumor growth in osteosarcoma. J Immunother Cancer. 2021 Mar;9(3): e001703.
PUBMED DOIGambera S, Patiño-Garcia A, Alfranca A, Garcia-Castro J RGB-Marking to Identify Patterns of Selection and Neutral Evolution in Human Osteosarcoma Models. Cancers . 2021 Apr 21;13(9):2003.
Gambera S, Patiño-Garcia A, Alfranca A, Garcia-Castro J RGB-Marking to Identify Patterns of Selection and Neutral Evolution in Human Osteosarcoma Models. Cancers . 2021 Apr 21;13(9):2003.
PUBMED DOIHermida-Prieto M., García-Castro J., Mariñas-Pardo L. Systemic treatment of immune-mediated keratoconjunctivitis sicca with allogeneic stem cells improves the schirmer tear test score in a canine spontaneous model of disease. Journal of Clinical Medicine. 2021; 10(24): 5981.
Hermida-Prieto M., García-Castro J., Mariñas-Pardo L. Systemic treatment of immune-mediated keratoconjunctivitis sicca with allogeneic stem cells improves the schirmer tear test score in a canine spontaneous model of disease. Journal of Clinical Medicine. 2021; 10(24): 5981.
PUBMED DOIMiguel Ángel Rodríguez-Milla, Alvaro Morales-Molina, Ana Judith Perisé-Barrios, Teresa Cejalvo, Javier García-Castro. AKT and JUN are differentially activated in mesenchymal stem cells after infection with human and canine oncolytic adenoviruses. Cancer Gene Therapy, 2021, 28, 64–73.
Miguel Ángel Rodríguez-Milla, Alvaro Morales-Molina, Ana Judith Perisé-Barrios, Teresa Cejalvo, Javier García-Castro. AKT and JUN are differentially activated in mesenchymal stem cells after infection with human and canine oncolytic adenoviruses. Cancer Gene Therapy, 2021, 28, 64–73.
PUBMED DOIAna Judith Perisé-Barrios, Beatriz Davinia Tomeo-Martín, Pablo Gómez-Ochoa, Pablo Delgado-Bonet, Pedro Plaza, Paula Palau-Concejo, Jorge González, Gustavo Ortiz-Díez, Antonio Meléndez-Lazo, Michaela Gentil, Javier García-Castro, Alicia Barbero-Fernández. Humoral responses to SARS-CoV-2 by healthy and sick dogs during the COVID-19 pandemic in Spain. Vet Res. 2021 Feb 15;52(1):22.4
Ana Judith Perisé-Barrios, Beatriz Davinia Tomeo-Martín, Pablo Gómez-Ochoa, Pablo Delgado-Bonet, Pedro Plaza, Paula Palau-Concejo, Jorge González, Gustavo Ortiz-Díez, Antonio Meléndez-Lazo, Michaela Gentil, Javier García-Castro, Alicia Barbero-Fernández. Humoral responses to SARS-CoV-2 by healthy and sick dogs during the COVID-19 pandemic in Spain. Vet Res. 2021 Feb 15;52(1):22.4
PUBMED DOIDavid Ruano, José A. López-Martín, Lucas Moreno, Álvaro Lassaletta, Francisco Bautista, Maitane Andión, Carmen Hernández, África González-Murillo, Gustavo Melen, Ramón Alemany, Luis Madero, Javier García-Castro, Manuel Ramírez First-in-Human, First-in-Child Trial of Autologous MSCs Carrying the Oncolytic Virus Icovir-5 in Patients with Advanced Tumors Mol Ther. 2020 Apr 8; 28(4): 1033–1042.
David Ruano, José A. López-Martín, Lucas Moreno, Álvaro Lassaletta, Francisco Bautista, Maitane Andión, Carmen Hernández, África González-Murillo, Gustavo Melen, Ramón Alemany, Luis Madero, Javier García-Castro, Manuel Ramírez First-in-Human, First-in-Child Trial of Autologous MSCs Carrying the Oncolytic Virus Icovir-5 in Patients with Advanced Tumors Mol Ther. 2020 Apr 8; 28(4): 1033–1042.
PUBMED DOIThomas GP Grünewald, Marta Alonso, Sofia Avnet, Ana Banito, Stefan Burdach, Florencia Cidre‐Aranaz,Gemma Di Pompo, Martin Distel, Heathcliff Dorado‐Garcia, Javier Garcia‐Castro, Laura González‐González, Agamemnon E Grigoriadis, Merve Kasan, Christian Koelsche, Manuela Krumbholz, Fernando Lecanda, Silvia Lemma, Dario L Longo, Claudia Madrigal‐Esquivel, Álvaro Morales‐Molina, Julian Musa, Shunya Ohmura, Benjamin Ory, Miguel Pereira‐Silva, Francesca Perut, Rene Rodriguez, Carolin Seeling, Nada Al Shaaili, Shabnam Shaabani, Kristina Shiavone, Snehadri Sinha, Eleni M Tomazou, Marcel Trautmann, Maria Vela,Yvonne MH Versleijen‐Jonkers, Julia Visgauss, Marta Zalacain, Sebastian J Schober, Andrej Lissat, William R English, Nicola Baldini, Dominique Heymann. Sarcoma treatment in the era of molecular medicine EMBO Mol Med 2020; 12(11):e11131.
Thomas GP Grünewald, Marta Alonso, Sofia Avnet, Ana Banito, Stefan Burdach, Florencia Cidre‐Aranaz,Gemma Di Pompo, Martin Distel, Heathcliff Dorado‐Garcia, Javier Garcia‐Castro, Laura González‐González, Agamemnon E Grigoriadis, Merve Kasan, Christian Koelsche, Manuela Krumbholz, Fernando Lecanda, Silvia Lemma, Dario L Longo, Claudia Madrigal‐Esquivel, Álvaro Morales‐Molina, Julian Musa, Shunya Ohmura, Benjamin Ory, Miguel Pereira‐Silva, Francesca Perut, Rene Rodriguez, Carolin Seeling, Nada Al Shaaili, Shabnam Shaabani, Kristina Shiavone, Snehadri Sinha, Eleni M Tomazou, Marcel Trautmann, Maria Vela,Yvonne MH Versleijen‐Jonkers, Julia Visgauss, Marta Zalacain, Sebastian J Schober, Andrej Lissat, William R English, Nicola Baldini, Dominique Heymann. Sarcoma treatment in the era of molecular medicine EMBO Mol Med 2020; 12(11):e11131.
PUBMED DOIAlvaro Morales-Molina, Miguel Ángel Rodríguez-Milla, Alicia Gimenez-Sanchez, Ana Judith Perisé-Barrios, Javier García-Castro. Cellular Virotherapy Increases Tumor-Infiltrating Lymphocytes (TIL) and Decreases their PD-1+ Subsets in Mouse Immunocompetent Models Cancers 2020 Jul; 12(7): 1920.
Alvaro Morales-Molina, Miguel Ángel Rodríguez-Milla, Alicia Gimenez-Sanchez, Ana Judith Perisé-Barrios, Javier García-Castro. Cellular Virotherapy Increases Tumor-Infiltrating Lymphocytes (TIL) and Decreases their PD-1+ Subsets in Mouse Immunocompetent Models Cancers 2020 Jul; 12(7): 1920.
PUBMED DOIAna Gómez, David Sardón, Teresa Cejalvo, Fernando Vázquez, Javier García-Castro, Ana Judith Perisé-Barrios. Biodistribution Analysis of Oncolytic Adenoviruses in Canine Patient Necropsy Samples Treated with Cellular Virotherapy Molecular Therapy: Oncolytics Vol. 18 September 2020: 525-534.
Ana Gómez, David Sardón, Teresa Cejalvo, Fernando Vázquez, Javier García-Castro, Ana Judith Perisé-Barrios. Biodistribution Analysis of Oncolytic Adenoviruses in Canine Patient Necropsy Samples Treated with Cellular Virotherapy Molecular Therapy: Oncolytics Vol. 18 September 2020: 525-534.
PUBMED DOI-

-

Sergio Casas Tintó
E. Científico Titular de OPIs (A3), Jefe de Unidad
ORCID code: 0000-0002-9589-9981
-

María José Barrero Núñez
E. Científico Titular de OPIs (A3), Jefe de Unidad
ORCID code: 0000-0002-5990-7040
-
Francisco Javier Alonso García de la Rosa
Profesor de Investigación de OPIs. Jefe de grupo
ORCID code: 0000-0002-6287-8391
-

-
Saint Thomas Cervera Mayor
Investigador predoctoral
-
-

Diana Sánchez Ponce
E. Ayudante de Investigación de OPIS I+D
-
-
-
Mario Santafé
Estudiante de doctorado
-

-

-
Silvia Méndez
Estudiante de doctorado
-
Iván Hernández-Martínez
Estudiante de doctorado
-
Déborah Gómez-Domínguez
Investigadora postdoctoral
-
-

-

-
Mª de los Ángeles Fernández Guijarro
Secretaria SITTE y SITE
UNIDAD DE INVESTIGACIÓN DE ANOMALÍAS CONGÉNITAS
List of staff
Información adicional
La Unidad de Modelos y Mecanismos tiene como objetivo la generación de modelos celulares para facilitar el diagnóstico de enfermedades raras complejas y estudiar los mecanismos moleculares responsables de la sintomatología de los pacientes. Entre otros modelos generamos células madre pluripotentes inducidas, también conocidas como iPSCs, a partir de células somáticas de pacientes con enfermedades raras que posteriormente diferenciamos a tipos celulares relevantes para estudiar la enfermedad, como por ejemplo neuronas. Nuestra unidad se centra especialmente (aunque no exclusivamente) en el estudio de enfermedades raras con base epigenética y en el uso de perfiles epigenéticos para mejorar el diagnóstico.
El Programa de Enfermedades Raras sin diagnostico – SpainUDP se desarrolla desde el Instituto de Investigación de Enfermedades Raras (IIER), perteneciente al ISCIII.
Dicho Programa intenta dar respuesta al elevado número de consultas que este centro viene recibiendo desde hace años sobre casos de enfermedades raras sin diagnóstico. SpainUDP ofrece un enfoque multidisciplinario a aquellos pacientes que llevan un prolongado periodo de tiempo buscando sin éxito un diagnóstico para su enfermedad.
¿Cómo contactar para solicitar entrar en el programa?
Existen dos posibilidades de acceso a este programa:
1. Registrándose en el registro de pacientes de enfermedades raras http://registroraras.isciii.es dejando la pestaña de diagnóstico como caso sin diagnóstico
2. A través del Sistema de Información y Orientación de Enfermedades Raras de FEDER
También se puede iniciar el primer contacto a través del correo registroraras@isciii.es
Este programa se realiza bajo la estrecha colaboración con la Red Internacional de Casos sin Diagnósticos (UDNI), la federación Española de Enfermedades Raras (FEDER), la Asociación D'Genes y la Asociación Objetivo Diagnóstico, cuyo Facebook puede seguirse en este enlace https://www.facebook.com/objetivodiagnostico/
Descripción del proceso
Análisis fenotípico
Durante la primera fase del protocolo se lleva a cabo un análisis del fenotipo clínico. Para ello:
· Se solicita la información clínica disponible de cada caso y todos los documentos son cuidadosamente revisados por los profesionales del Programa. La información clínica de los pacientes se almacena de forma segura en el Registro Nacional de Enfermedades Raras, previa firma del correspondiente consentimiento informado.
· Se establece una estrecha colaboración con los servicios médicos locales que atienden a los pacientes
· Si es necesario, los pacientes admitidos en el programa son citados en consultas externas, o bien ingresados en el Hospital Universitario Puerta de Hierro de Majadahonda (Madrid) para realizar un estudio clínico detallado de dichos pacientes, así como las pruebas diagnósticas que se consideren necesarias para completar la valoración de su estado clínico
Estudios genéticos
· Durante esta fase, toda la información procedente de los estudios genéticos realizados en otros centros es analizada, llegando en caso de considerarlo necesario, a contactar con el laboratorio que ha llevado a cabo dicho estudio genético con el objetivo de validar conjuntamente tanto los hallazgos como la falta de los mismos.
· Cualquier decisión acerca de decisiones a tomar sobre repetición/comprobación de análisis ya realizados, se lleva a cabo en estrecha colaboración con la familia, pero también con sus médicos.
· Por último, si el caso lo requiere se procede a realizar un estudio del exoma completo del caso, de los padres y si lo consideramos de interés en los hermanos del caso. Para este análisis se requiere la firma de un nuevo consentimiento informado ad hoc para estudios de este tipo.
· Para la realización del exoma, se requieren muestras de sangre, muestras que se obtienen siguiendo el procedimiento estandarizado por el Biobanco Nacional de Enfermedades Raras ISCIII (BioNER), con la consiguiente firma de un consentimiento informado que permite guardar la parte de la muestra no utilizada en el diagnóstico en el propio biobanco. Estas muestras podrán ser utilizadas para comprobaciones de análisis diagnósticos y para estudios funcionales demostrativos de que la mutación(es) encontrada(s) son la causa de la enfermedad.
Fase de información
· El informe completo del exoma es enviado tanto al médico del caso como a la propia familia. Los médicos de cada caso son los que finalmente proceden a valorar los hallazgos, los discuten con el IIER, si lo consideran necesario, y son los encargados de transmitir y firmar el diagnóstico definitivo al caso o a la familia (en caso de menores o incapacitados).
· El informe genético se envía a la familia para que puedan entregarlo en caso de terceras opiniones o desplazamientos de lugar de residencia.
¿Qué pasa si el estudio del exoma no detecta ninguna mutación capaz de relacionarse con el cuadro clínico?
Aproximadamente 1 de cada dos estudios de este tipo se encuentra en esta situación, es decir, no se alcanza un diagnóstico claro. Para ello se está colaborando con la Red Internacional de Casos sin Diagnóstico http://www.udninternational.org/ y con los proyectos europeos RD-CONNECT y SOLVE-RD, recientemente aprobado precisamente para ver la manera de solucionar el diagnóstico de estas personas entre todos.
La idea es buscar casos similares en todo el mundo, a través de la compartición de datos del fenotipo clínico – debidamente mapeado con la Ontología de Fenotipo Humano – y datos de variantes genéticas candidatas. Todo este vasto proceso, que está comenzando a lanzarse muy recientemente a través de plataformas de intercambio seguras como Phenome Central, Matchmaker Exchange y desde RD-CONNECT permitirá abordar diferencias y similitudes entre casos de distinto origen, permitirán conocer mejor los mecanismos de las enfermedades complejas y facilitará el diagnóstico de muchos más casos.
Servicio de Información Telefónica para la Embarazada (SITE)
Teléfono: 91 822 24 36 (para la población general).
Horario de consultas: 9 a 15 horas (lunes a viernes)

La información que se ofrece en el SITE está especialmente dirigida a:
- Las mujeres embarazadas y sus parejas.
- Las parejas que planean una gestación.
- Los padres que han tenido previamente un hijo (o un embarazo) con algún defecto congénito.
En este servicio se puede consultar sobre el riesgo que para defectos congénitos puede implicar la exposición a cualquier factor u otros aspectos que les puedan preocupar a ese respecto (tales como: edades de los padres, tabaco, alcohol, drogas, exposiciones laborales maternas o paternas, contacto con animales domésticos, etc). Para problemas médicos o tratamientos, la consulta debe realizarla el profesional encargado del cuidado de la paciente.
En cada llamada, además se ofrece información general sobre medidas preventivas para defectos congénitos, que se envía por correo a todas aquellas personas que lo soliciten.
Servicio de Información Telefónica sobre Teratógenos Español (SITTE)
Teléfono: 91 822 24 35 (para profesionales sanitarios).
Horario de consultas: 9 a 15 horas (lunes a viernes)

Este servicio tiene una finalidad equivalente a la del SITE, pero está dirigido a profesionales de la salud. Todas las consultas sobre problemas médicos o tratamientos deben ser canalizadas a través del SITTE.
Se conoce como enfermedad rara (ER) aquella cuya prevalencia es inferior a 5 casos por cada 10.000 personas en la Comunidad Europea. El objetivo del Registro de Pacientes de Enfermedades Raras es ofrecer a los profesionales del sistema de salud, investigadores, y al colectivo de pacientes y familiares un mayor nivel de conocimiento acerca del número y distribución geográfica de las personas afectadas por ER en España. Se persigue así fomentar la investigación y aumentar la visibilidad de estas enfermedades, y favorecer la toma de decisiones para una adecuada planificación sanitaria y una correcta distribución de recursos.
El Registro de Pacientes de Enfermedades Raras tiene dos vías principales de entrada de información (casos): 1) a partir de la inclusión directa del paciente por parte del propio afectado o de un familiar o representante en https://registroraras.isciii.es/ y, 2) mediante los profesionales que incluyan la información de sus bases de datos (ya sean investigadores o sociedades médicas).

El registro se sustenta desde el punto de vista legal en la orden publicada en el B.O.E de junio de 2005, (ORDEN SCO/1730/2005, DE 31 DE MAYO), donde se establecieron los criterios de creación y funcionamiento, el lugar dónde debe estar depositada la custodia legal y la responsabilidad del mismo, y sobre su mantenimiento y ulterior desarrollo. Al mismo tiempo, este registro ha sido declarado de carácter oficial ante la Agencia Nacional de Protección de Datos, en cumplimiento de la normativa vigente relativa a la protección de datos personales con el número 2060180217.
Orientado a personas afectadas y sus familias:
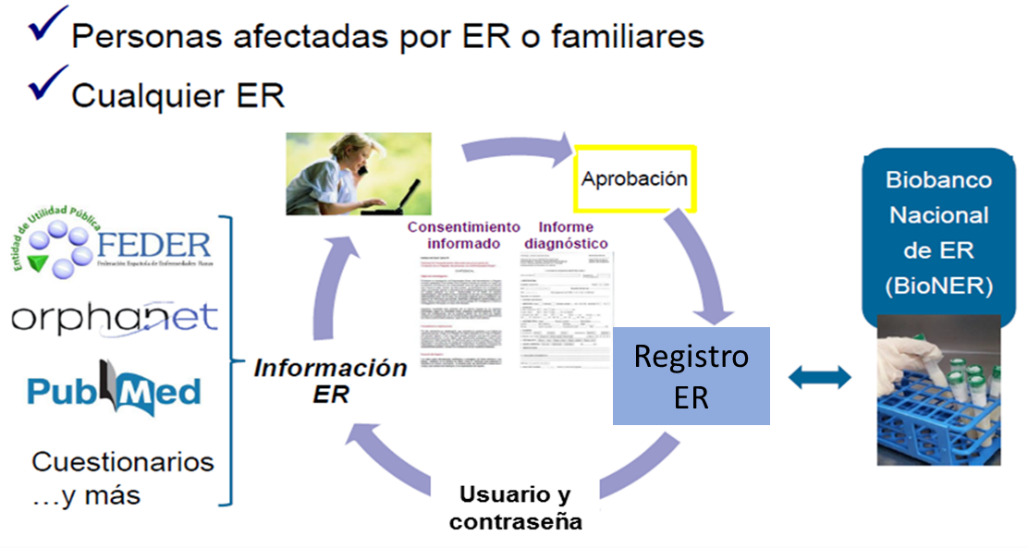
Cualquier persona afectada por ER, o familiar, puede inscribirse de forma voluntaria en el Registro de Pacientes de Enfermedades Raras.
Se ofrece a los propios pacientes o tutores (en caso de niños y personas incapacitadas) la oportunidad de inscribirse en este registro a través de la página web https://registroraras.isciii.es/. Una vez validada la solicitud, se proporciona un usuario y contraseña para que la persona inscrita pueda acceder al registro, consultar información sobre su enfermedad y participar en estudios mediante cuestionarios on-line sobre: uso de medicamentos, calidad de vida, análisis de la dependencia, recursos sanitarios, etc. Además, se ofrece la posibilidad de donar muestras biológicas, por su conexión con el Biobanco Nacional de Enfermedades Raras (BioNER).
Orientado a profesionales:
Los profesionales con experiencia en alguna enfermedad rara, con registros de pacientes ya existentes o con interés en desarrollar un nuevo registro, también pueden colaborar con el Registro de Pacientes de Enfermedades Raras y unificar esfuerzos.
Los registros de pacientes que colaboran mantienen su identidad, autonomía y gestión de datos y, al tiempo que se benefician de formar parte del Registro de Enfermedades Raras, se favorece la investigación, optimizan los recursos y respetan los derechos de los ciudadanos.
La incorporación de registros de pacientes a una red de investigación conlleva VENTAJAS como la reducción de costes, promoción, difusión y menor fragmentación del número de casos.
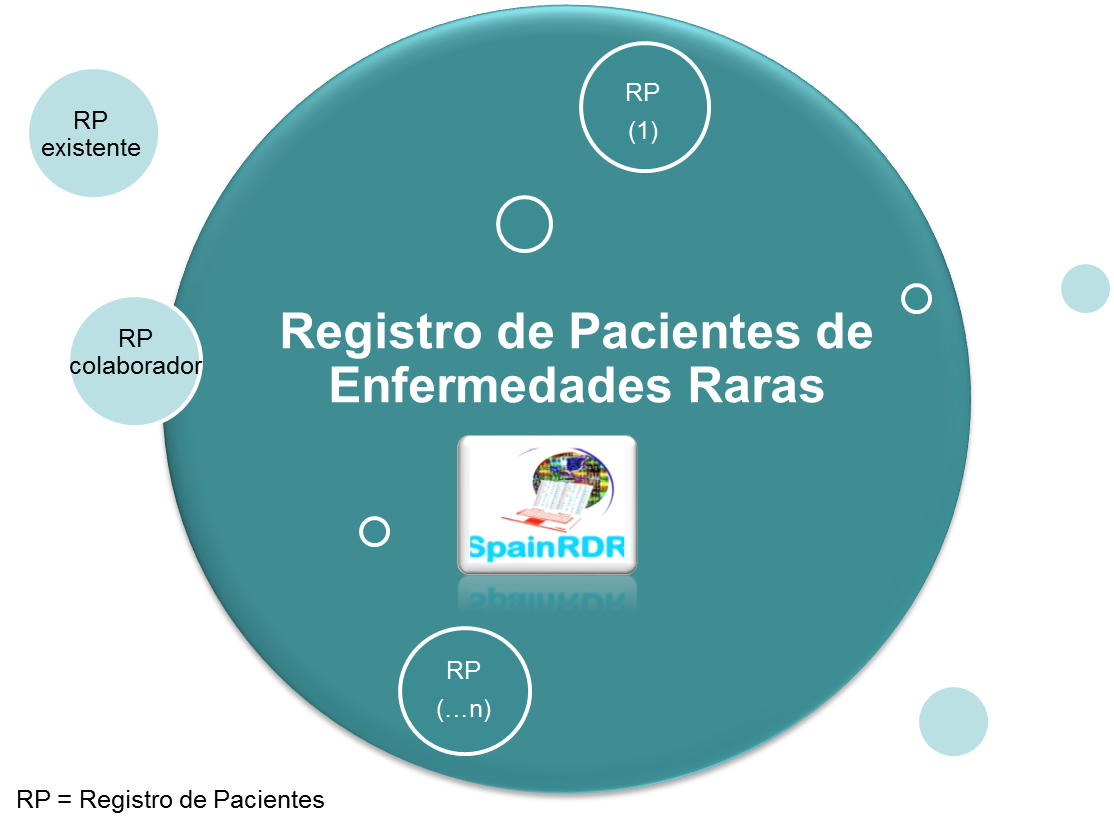
El Registro de Pacientes de Enfermedades Raras del ISCIII surge de la red de registros SpainRDR ofreciendo posibilidades de colaboración, sin menoscabo de la identidad o autonomía de cada registro.
Procedimiento de colaboración e incorporación de registros de pacientes:
- Con cada Sociedad o Grupo de investigación se firma un Convenio de colaboración con el Instituto de Investigación de Enfermedades Raras (IIER), Instituto de Salud Carlos III
- El compromiso de los profesionales participantes se manifiesta en un Acuerdo de Consorcio
- Se define el Modelo de datos en colaboración con los responsables, manteniendo la interoperabilidad entre registros de pacientes
- Se facilita el Consentimiento informado ya evaluado y aceptado por el Comité de Ética del IIER
- El Registro de Pacientes de ER está declarado en la Agencia Española de Protección de Datos, por lo que cualquier registro que se integre en él no precisaría una declaración propia
- Se facilita el Documento de seguridad del Registro de Pacientes de ER para mantener la confidencialidad
- Autorización de Acceso al registro mediante usuario y contraseña. Existen diferentes permisos de forma que cada grupo tendrá únicamente acceso a la información de los pacientes de su registro.
Si desea iniciar una colaboración, por favor escriba a: registro.raras@isciii.es